Энергообеспечение мышечной деятельности
Содержание:
- Суммарный выход гликолиза
- Аэробный режим энергообеспечения мышечной деятельности
- Регулирование гликолиза
- Распространение и значение
- Этапы окислительного гликолиза. Фаза 1.
- Примечания и ссылки
- Почему пируват, а не другая молекула?
- Бескислородное окисление глюкозы включает два этапа
- Гликолиз в раковых клетках
- История исследования
- Основные отличия дихотомического анаэробного распада глюкозы и аэробного гликолиза
- Фаза 2. Синтез Адезинтрифосфата
- 6-я ступень – окисление глицеральдегид-3-фосфата
- 7-я ступень. Перемещение фосфатной группы с 1,3-дифосфоглицерата на адезиндифосфат
- 8-я ступень. Перенесение фосфорильной группы с 3-фосфоглицерата.
- 9-я ступень. Выделение воды из 2-фосфоглицерата
- 10-я и последняя ступень. Перенос фосфатного остатка с ФЕП на АДФ
- Что такое гликолиз
- Что такое анаэробный гликолиз?
Суммарный выход гликолиза
| Изменение свободной энергии в реакциях гликолиза в эритроцитах | ||
|---|---|---|
| Реакция | ΔG 0 (кДж / моль) | ΔG (кДж / моль) |
| Глюкоза + АТФ → глюкозо-6-фосфат + АДФ | -16,7 | -33,4 |
| Глюкозо-6-фосфат фруктозо-6-фосфат | 1,7 | от 0 до 25 |
| Фруктозо-6-фосфат + АТФ → фруктозо-1,6-бисфосфат + АДФ | -14,2 | -22,2 |
| Фруктозо-1,6-бисфосфат глицеральдегид-3-фосфат + дигидроксиацетонфосфат | 28,3 | от -6 до 0 |
| Дигидроксиацетонфосфат глицеральдегид-3-фосфат | 7,5 | от 0 до 4 |
| Глицеральдегид-3-фосфат + Ф н + НАД + 1,3-бисфосфоглицерат + НАДH + H + | 6,3 | от -2 до 2 |
| 1,3-бисфосфоглицерат + АДФ 3-фосфоглицерат + АТФ | -18,8 | от 0 до 2 |
| 3-фосфоглицерат 2-фосфоглицерат | 4,4 | от 0 до 0,8 |
| 2-фосфоглицерат фосфоэнолпируват + H 2 O | 7,5 | от 0 до 3,3 |
| Фосфоэнолпируват + АДФ → пируват + АТФ | -31,4 | -16,7 |
Общее уравнение гликолиза имеет следующий вид:
Глюкоза + 2Ф н + 2АДФ + 2НАД + → 2 пируват + 2АТФ + 2НАДН + 2Н + + 2Н 2 О.
Суммарное количество энергии, выделяющейся в процессе расщепления глюкозы до пирувата составляет 146 кДж / моль, на синтез двух молекул АТФ расходуется 61 кДж / моль, остальные 85 кДж / моль энергии превращается в тепло.
При полном окислении глюкозы до углекислого газа и воды выделяется 2840 кДж / моль, если сравнить это значение с общим выходом екзергоничних реакций гликолиза (146 кДж / моль), то становится понятно, что 95% энергии глюкозы остается «заключенной» в молекулах пирувата. Хотя реакции гликолиза являются универсальными почти для всех организмов, дальнейшая судьба его продуктов — пирувата и НАДН — отличается в разных живых существ и зависит от условий.
В аэробных организмов при достаточной концентрации кислорода НАД + регенерируется путем передачи электронов в дыхательная цепь переноса электронов, который в эукариот расположен во внутренней мембране митохондрий. Конечным акцептором электронов при этом является кислород. Пируват подвергается окислительного декарбоксилирования, превращается в ацетил-КоА и поступает в цикл Кребса, где происходит его дальнейшее окисление. Отщеплений электроны также попадают в дыхательная цепь переноса электронов.
С другой стороны, в анаэробных условиях восстановлен НАДH не может передать свои электроны на кислород, поэтому он переносит их или непосредственно назад на молекулу пирувата, как в процессе молочнокислого брожения, или на определенные продукты его превращения, например в ацетальдегид в случае спритового брожения. Анаэробный метаболизм глюкозы дает значительно меньше энергии, чем аэробный.
Аэробный режим энергообеспечения мышечной деятельности
Если при гликолизе исходным продуктом выработки энергии служат исключительно углеводы, то при аэробном режиме энергообеспечения мышечной деятельности организм использует все компоненты питания – углеводы, белки, жиры. Именно при аэробном процессе организм добывает энергии почти в двадцать раз больше, нежели при гликолизе. Причем конечные продукты реакций здесь практически нейтральны – вода и углекислый газ, который выводится из организма при дыхании.
На этот счет образное сравнение сделал всемирно известный биохимик А. Ленинджер. Если первые два пути ресинтеза АТФ (анаэробные режимы) он сравнил с работой поршневого двигателя, то третий путь – аэробный, – он приравнял к тяге двигателя ракетного.
Итак, существуют как бы три уровня энергообеспечения мышечной деятельности. Но помните, как сказано выше, использования креатинфосфата хватает на 10 – 15 секунд работы, гликолиза на 2 – 4 минуты… Способность человека к ресинтезу АТФ в данных случаях совершенно индивидуальны. Точно так же индивидуальны они и при аэробном механизме. С одной стороны, мощность и емкость (есть такие термины) каждого уровня обусловлены природой, с другой – диапазон каждого из них может быть расширен за счет тренировки.
Все это хорошо, скажет читатель recipehealth.ru, но каким образом, где претерпевают все превращения на пути к ресинтезу АТФ белки, жиры и углеводы. Представьте, для этого в каждой клетке есть своего рода энергетические подстанции. Название им – митохондрии. В недрах митохондрий и происходит беспрерывный процесс восстановления АТФ. И этот процесс идет в аэробном режиме.
В обычных условиях «работает» лишь часть митохондрий. Но по мере потребности мышц в энергии в процесс ресинтеза АТФ включается все больше и больше подстанций. Наконец, за дело берутся все! Но энергии для обеспечения мышечной деятельности нужно еще больше…
Вот так выглядит митохондрия (компьютерная инсталяция)
Митохондрии, как и все клетки организма, живут и отмирают. Идет постоянный процесс их обновления. Но вот в чем хитрость. Когда запросы организма в АТФ для энергообеспечения мышечной деятельности все возрастают, в клетках увеличивается и число митохондрий. Когда же и это число уже перестает удовлетворять запросы, убыстряется темп обновления.… Именно этот процесс имелся в виду, когда говорилось о том, что диапазон каждого энергетического уровня можно расширить за счет тренировки.
Вот, пожалуй, очень короткий и, конечно, весьма упрощенный взгляд на проблему энергообеспечения мышечной деятельности организма. Надеюсь, что понимание этого процесса, даже на изложенном уровне, поможет вам в выборе пути укрепления здоровья, расширив диапазон знаний о самом себе. Это был намек, а теперь, дорогие друзья, я призываю открытым текстом: увеличивайте количество своих митохондрий и скорость их обновления, используя информацию из рубрики «Спортзал»!
А вот что рассказывает о биохимических основах мышечной деятельности химик:
Регулирование гликолиза
Гликолиз в основном регулируется на уровне трех ключевых ферментов: PFK-1 , пируваткиназы и гексокиназы .
Регламент ПФК-1
ПФК-1 управляется таким образом аллостерическим :
- АТФ и цитрат действуют как ингибиторы
- AMP и фруктоза 2,6-бисфосфат действует в качестве активаторов.
Следовательно, концентрация фруктозо-2,6-бисфосфата важна для гликолиза. Он регулируется фосфофруктокиназой-2, активность которой различается в зависимости от состояния фосфорилирования:
- под действием инсулина ( гипогликемического гормона ) он дефосфорилируется и катализирует реакцию фруктозо-6-фосфат + АТФ → фруктоза-2,6-бисфосфат + АДФ ; увеличивается концентрация фруктозо-2,6-бисфосфата и ускоряется гликолиз.
- под действием глюкагона (гипергликемического гормона) фосфорилируется и катализирует реакцию: фруктозо-2,6-бисфосфат + H 2 O→ фруктозо-6-фосфат + Pi ; снижается концентрация фруктозо-2,6-бисфосфата и замедляется гликолиз.
Регулирование пируваткиназы
Пируваткиназы регулируется аллостерически и это Повсеместно:
- AMP и фруктозо-1,6-дифосфат являются активаторы
- АТФ , то ацетил-КоА и аланин являются ингибиторами.
В печени он также регулируется ковалентно (действием гормонов ).
- глюкагона действует путем фосфорилирования этого фермента , который обладает эффектом ингибирования
- что инсулин выполняет обратное действие, которое оказывает эффект активирующих пируваткиназ.
Регулирование гексокиназы
Активность этого фермента подавляется продуктом реакции глюкозо-6-фосфатом . Если он накапливается, его производство быстро снижается, чтобы сбалансировать его потребление. Этот процесс предотвращает накопление метаболитов .
Распространение и значение
Гликолиз является почти универсальным для всех клеточных организмов путем катаболизма глюкозы. Вероятно, он возник на ранних этапах развития жизни на Земле, еще до того, как в атмосфере накопился кислород в результате деятельности фотосинтезирующих организмов. Последовательность гликолитических реакций — чрезвычайно эволюционно консервативный путь. Ферменты, которые принимают в нем участие, проявляют высокую степень гомологии как в аминокислотной последовательности, так и трехмерной структуре у позвоночных животных, дрожжей и растений. Как показало секвенирования ДНК геномов большого количества организмов, только в некоторых архей и паразитических бактерий отсутствуют один или несколько ферментов гликолиза, несмотря на то, что сам путь сохраняется, вероятно, в модифицированном виде.
В эукариотических клетках реакции гликолиза происходят в цитозоле. В большинстве таких клеток именно этот среди других метаболических путей занимает первое место по количеству атомов углерода, которые превращаются в нем. Для таких тканей млекопитающих, как мозг (за исключением условий голодания), мозговой слой почек, сперматозоиды, а также эритроциты, в которых полностью отсутствуют митохонондрии, гликолиз является единственным источником метаболической энергии. Для мышц в условиях очень большой нагрузки гликолиз выгоден не только потому, что дает возможность получить энергию при недостатке кислорода, а еще и потому, что он происходит очень быстро и обеспечивает синтез АТФ в 10,5 раз быстрее, чем аэробная окисления органических веществ . Также от гликолиза главным образом зависят растительные ткани, специализированные на хранении крахмала (например клубни картофеля), и водные растения, такие как настурция лекарственная.
Другими путями окисления глюкозы является пентозофосфатный путь и путь Энтнера-Дудорова. Последний является заменой гликолиза в некоторых грамотрицательных и, очень редко, грамположительных бактерий и имеет много общих черт с ним ферментов.
Этапы окислительного гликолиза. Фаза 1.
В аэробном гликолизе выделяются 2 фазы.
Первая фаза – подготовительная. В ней глюкоза вступает в реакцию с 2 молекулами АТФ. Эта фаза состоит из 5 последовательных ступеней биохимических реакций.
1-я ступень. Фосфорилирование глюкозы
Фосфорилирование, то есть процесс переноса остатков фосфорной кислоты в первой и последующих реакциях производится за счет молекул адезинтрифосфорной кислоты.
В первой ступени остатки фосфорной кислоты из молекул адезинтрифосфата переносятся в молекулярную структуру глюкозы. В ходе процесса получается глюкозо-6-фосфат. В качестве катализатора в процессе выступает гексокиназа, ускоряющая процесс с помощью ионов магния, выступающих в качестве кофактора. Ионы магния задействованы и в других реакциях гликолиза.

2-я ступень. Образование изомера глюкозо-6-фосфата

На 2-й ступени происходит изомеризация глюкозо-6-фосфата во фруктозу-6-фосфат.
Изомеризация – образование веществ, имеющих одинаковый вес, состав химических элементов, но обладающих разными свойствами вследствие различного расположения атомов в молекуле. Изомеризация веществ осуществляется под действием внешних условий: давления, температур, катализаторов.
В данном случае процесс осуществляется под действием катализатора фосфоглюкозоизомеразы при участии ионов Mg+.
3-я ступень. Фосфорилирование фруктозо-6-фосфата
На данной ступени происходит присоединение фосфорильной группы за счет АТФ. Процесс осуществляется при участии фермента фосфофруктокиназа-1. Этот фермент и предназначен только для участия в гидролизе. В результате реакции получаются фруктозо-1,6-бисфосфат и нуклеотид адезинтрифосфат.

АТФ – адезинтрифосфат, уникальный источник энергии в живом организме. Представляет собой довольно сложную и громоздкую молекулу, состоящую из углеводородных, гидроксильных групп, азота и групп фосфорной кислоты с одной свободной связью, собранных в нескольких циклических и линейных структурах. Высвобождение энергии происходит в результате взаимодействия остатков фосфорной кислоты с водой. Гидролиз АТФ сопровождается образованием фосфорной кислоты и выделением 40-60 Дж энергии, которую организм затрачивает на свою жизнедеятельность.
Но прежде должно произойти фосфорилирование глюкозы за счет молекулы Адезинтрифосфата, то есть перенос остатка фосфорной кислоты в глюкозу.
4-я ступень. Распад фруктозо-1,6-дифосфата

В четвертой реакции фруктозо-1,6-дифосфат распадается на два новых вещества.
- Диоксиацетонфосфат,
- Глицеральд альдегид-3-фосфат.
В данном химическом процессе в качестве катализатора выступает альдолаза, фермент, участвующий в энергетическом обмене, и необходимый при диагностировании ряда заболеваний.
5-я ступень. Образование триозофосфатных изомеров
И, наконец, последний процесс – изомеризация триозофосфатов.

Глицеральд-3-фосфат продолжит участвовать в процессе аэробного гидролиза. А второй компонент – диоксиацетон фосфат при участии фермента триозофосфатизомеразы преобразуется в глицеральдегид-3-фосфат. Но трансформация эта – обратимая.
Примечания и ссылки
- Стивен Д. Антон , Keelin Moehl , Уильям Т. Донахью и Krisztina Marosi , « Подавать метаболический переключатель: Понимание и применение Польза для здоровья Голодание », Ожирение (. Silver Spring, MD) , Vol. 26, п о 2февраль 2018, стр. 254–268
- ↑ и (in) Реджинальд Х. Гарретт и Чарльз М. Гришем , Биохимия , Wadsworth Publishing Co Inc.,2012 г., 5- е изд. , 1280 с.
- Паскаль Риберо-Гайон , Дени Дюбурдье , Бернар Донеш и Алин Лонво , Договор об энологии , т. 1: Микробиология вина. Виноделие , Данод,3 октября 2012 г., 6- е изд. ( ISBN 978-2-10-058234-1 и 2-10-058234-8 )
-
(in) HS Seeholzer, A. Jaworowski, IA Rose , Энолпируват: химическое определение как промежуточное соединение пируваткиназы , Biochemistry , vol. 30, п о 3,
22 января 1991 г., стр. 727-732 -
Джордж Б. Джонсон , Джонатан Б. Лосос , Питер Х. Рэйвен и Сьюзан С. Сингер ( перевод с англ.), Биология: роскошная версия , Брюссель / Париж, Superior De Boeck
15 ноября 2009 г., 1406 с. ( ISBN 978-2-8041-6638-0 ) -
Жозеф-Пьер Гиро , Пищевая микробиология , Dunod,
18 сентября 2012 г., 2- е изд. ( ISBN 978-2-10-057008-9 и 2-10-057008-0 )
Почему пируват, а не другая молекула?
Наш организм получает энергию из белков, жиров и углеводов. Можно подумать, что для каждого класса молекул существует отдельный способ вытащить из него энергию. Но это не так. Зачем делать печку для каждого вида дров, если можно сделать одну общую для всех? Таким вопросом задались клетки нашего организма и решили, что лучше сделать одну печь. Эта печь — общий путь катаболизма.
Общий путь катаболизма включает превращение пирувата в ацетил-коэнзим А, цикл трикарбоновых кислот и цепь переноса электронов. Видите? Он начинается с пирувата. Потому что:
Клетки умнее, чем кажутся. Они решили, что можно сделать не только одну печь, но и один вид дров. Они окисляют белки, жиры и углеводы до одной молекулы — ацетил-коэнзим А. И пируват — это его предшественник. Их отделяет всего одна реакция, поэтому если мы посмотрим на все виды обмена, то увидим такое.
Общий путь катаболизма
В ходе общего пути катаболизма образуется огромное количество молекул АТФ. Куда больше, чем при гликолизе.
Теперь мы поняли, что гликолиз — это первый этап катаболизма глюкозы. В ходе него образуется немного энергии в виде АТФ. Но что важнее — гликолиз готовит дрова для печи. Или пируват для общего пути катаболизма, как тебе больше нравится.
У гликолиза есть и другое название — дихотомическое расщепление глюкозы. Это название заключает главный смысл гликолиза: в ходе него происходит деление молекулы глюкозы надвое.
Бескислородное окисление глюкозы включает два этапа

В анаэробном процессе пировиноградная кислота восстанавливается до молочной кислоты (лактата), поэтому в микробиологии анаэробный гликолиз называют молочнокислым брожением. Лактат является метаболическим тупиком и далее ни во что не превращается, единственная возможность утилизовать лактат – это окислить его обратно в пируват.
Многие клетки организма способны к анаэробному окислению глюкозы. Для эритроцитов он является единственным источником энергии.
Клетки скелетной мускулатуры за счет бескислородного расщепления глюкозы способны выполнять мощную, быструю, интенсивную работу, как, например, бег на короткие дистанции, напряжение в силовых видах спорта.
Вне физических нагрузок бескислородное окисление глюкозы в клетках усиливается при гипоксии – при различного рода анемиях, при нарушении кровообращения в тканях независимо от причины.
Первый этап гликолиза – подготовительный, здесь происходит затрата энергии АТФ, активация глюкозы и образование из нее триозофосфатов.
Первая реакция гликолиза сводится к превращению глюкозы в реакционно-способное соединение за счет фосфорилирования 6-го, не включенного в кольцо, атома углерода. Эта реакция является первой в любом превращении глюкозы, катализируется гексокиназой.
Вторая реакция необходима для выведения еще одного атома углерода из кольца для его последующего фосфорилирования (фермент глюкозофосфат-изомераза). В результате образуется фруктозо-6-фосфат.
Третья реакция – фермент фосфофруктокиназа фосфорилирует фруктозо-6-фосфат с образованием почти симметричной молекулы фруктозо-1,6-дифосфата. Эта реакция является главной в регуляции скорости гликолиза.
В четвертой реакции фруктозо-1,6-дифосфат разрезается пополам фруктозо-1,6-дифосфат-альдолазой с образованием двух фосфорилированных триоз-изомеров – альдозы глицеральдегида (ГАФ) и кетозы диоксиацетона (ДАФ).
Пятая реакция подготовительного этапа – переход глицеральдегидфосфата и диоксиацетонфосфата друг в друга при участии триозофосфатизомеразы. Равновесие реакции сдвинуто в пользу диоксиацетонфосфата, его доля составляет 97%, доля глицеральдегидфосфата – 3%. Эта реакция, при всей ее простоте, определяет дальнейшую судьбу глюкозы:
- при нехватке энергии в клетке и активации окисления глюкозы диоксиацетонфосфат превращается в глицеральдегидфосфат, который далее окисляется на втором этапе гликолиза,
- при достаточном количестве АТФ, наоборот, глицеральдегидфосфат изомеризуется в диоксиацетонфосфат, и последний отправляется на синтез жиров.
Второй этап гликолиза – это освобождение энергии, содержащейся в глицеральдегидфосфате, и запасание ее в форме АТФ.
Шестая реакция гликолиза (фермент глицеральдегидфосфат-дегидрогеназа) – окисление глицеральдегидфосфата и присоединение к нему фосфорной кислоты приводит к образованию макроэргического соединения 1,3-дифосфоглицериновой кислоты и НАДН.
В седьмой реакции (фермент фосфоглицераткиназа) энергия фосфоэфирной связи, заключенная в 1,3-дифосфоглицерате тратится на образование АТФ.
Реакция получила дополнительное название – реакция субстратного фосфорилирования, что уточняет источник энергии для получения макроэргической связи в АТФ (от субстрата реакции) в отличие от окислительного фосфорилирования (от электрохимического градиента ионов водорода на мембране митохондрий).
Восьмая реакция – синтезированный в предыдущей реакции 3-фосфоглицерат под влиянием фосфоглицератмутазы изомеризуется в 2-фосфоглицерат.
Девятая реакция – фермент енолаза отрывает молекулу воды от 2-фосфоглицериновой кислоты и приводит к образованию макроэргической фосфоэфирной связи в составе фосфоенолпирувата.
Десятая реакция гликолиза – еще одна реакция субстратного фосфорилирования – заключается в переносе пируваткиназой макроэргического фосфата с фосфоенолпирувата на АДФ и образовании пировиноградной кислоты.
Последняя реакция бескислородного окисления глюкозы, одиннадцатая – образование молочной кислоты из пирувата под действием лактатдегидрогеназы
Важно то, что эта реакция осуществляется только в анаэробных условиях. Эта реакция необходима клетке, так как НАДН, образующийся в 6-й реакции, в отсутствие кислорода не может окисляться в митохондриях
| У плода и детей первых месяцев жизни преобладает анаэробный распад глюкозы, в связи с чем концентрация молочной кислоты в крови у них выше чем у взрослых. |
| При наличии кислорода пировиноградная кислота переходит в митохондрию и превращается в ацетил-S-КоА. |
Гликолиз в раковых клетках
1928 Отто Варбург обнаружил, что в раковых клетках почти всех типов гликолиз и поглощение глюкозы происходит примерно в 10 раз интенсивнее, чем у здоровых, даже в присутствии больших концентраций кислорода. Эффект Варбурга стал основой для разработки нескольких методов выявления и лечения рака.
Все раковые клетки, по крайней мере на начальных этапах развития опухоли растут в условиях гипоксии, то есть недостатка кислорода, из-за отсутствия сетки капилляров. Если они расположены на расстоянии более 100-200 мкм от ближайшей кровеносного сосуда, то должны полагаться только на гликолиз без дальнейшего окисления пирувата для получения АТФ. Йомвирно, что почти во всех раковых клетках в процессе злокачественной трансформации происходят следующие изменения: переход на получение энергии только путем гликолиза и приспособления к условиям повышенной кислотности, возникающих вследствие выделения молочной кислоты в межклеточную жидкость. Чем более агрессивная опухоль, тем быстрее в ней происходит гликолиз.
Приспособление раковых клеток к недостатку кислорода во многом происходит благодаря транскрипционных факторов индуцированном гипоксией (англ. Hypoxia-inducible transcription factor, HIF-1), который стимулирует повышение экспрессии как минимум восьми генов гликолитических ферментов, а также транспортеров глюкозы GLUT1 и GLUT3, активность которых не зависит от инсулина. Еще одним ефекторм HIF-1 является выделение клетками васкулярного эндотелиального фактора роста (англ. Vascular endothelial growth factor), что стимулирует образование кровеносных сосудов в опухоли. HIF-1 также выделяется мышцами во время тренировок, предусматривающие большую интенсивность нагрузки, в этом случае он имеет аналогичный эффект: усиливает способность к анаэробного синтеза АТФ и стимулирует рост капилляров.
В некоторых случаях повышенная интенсивность гликолиза может быть использована для нахождения местоположения опухоли в организме с помощью позитрон-эмиссионной томографии (ПЭТ). Пациенту в кровь вводят аналог глюкозы 2-флюоро-2-дезоксиглюкозу (ФДГ), меченый изотопом 18 F. Это вещество поглощается клетками и является субстратом для первого фермента гликолиза — гексокиназы, однако не может быть преобразована фосфоглюкоизмеразою, поэтому накапливается в цитоплазме. Скорость накопления зависит от интенсивности захвата аналога глюкозы и его фосфорилирования, оба процесса значительно быстрее происходят в раковых клетках, чем в здоровых. При распаде 18 F выделяются позитроны, которые фиксируются специальными сенсорами.
Особенности катаболизма глюкозы в злокачественных опухолях используются не только для диагностики, но и для разработки новых противораковых препаратов, среди которых: ингибиторы гексокиназы (2-дезоксиглюкоза, лонидамин, 3-бромпируват), Иматиниб (Gleevec), подавляющее определенную тирозинкиназы, которая стимулирует синтез гексокиназы, и другие.
История исследования
Гликолиз первый из открытых и наиболее исследован метаболический путь. 1897 братья Ганс и Эдуард Бюхнер занимались изготовлением бесклеточной экстрактов дрожжей для терапевтического применения. Очевидно, они не могли использовать ядовитые для человека антисептики, как фенол, поэтому попытались распространен в кулинарии консервант — сахарозу. Выяснилось, что в дрожжевых экстрактах это вещество быстро зброджувалась к этиловому спирту. Так впервые установлено, что брожение может происходить вне живых клеток. В 1907 году Эдуарду Бюхнеру была присуждена Нобелевская премия по химии.
Со времени открытия внеклеточного брожения до 1940-х годов исследования реакций гликолиза было одной из основных задач биохимии. Описанием этого метаболического пути в клетках дрожжей занимались Отто Варбург, Ганс фон Эйлер-Хельпин и Артур Гарден (два последних получили Нобелевскую премию по химии 1929 года), в мышцах — Густав Эмбден и Отто Меергоф (Нобелевская премия по медицине и физиологии 1922 ). Также свой вклад в исследование гликолиза сделали Карл Нойберг, Яков Парнас, Герти и Карл Кори.
Важными «побочными» открытиями, сделанными благодаря изучению гликолиза, была разработка многих методов очистки ферментов, выяснения центральной роли АТФ и других фосфорильованих соединений в метаболизме, открытие коэнзимов, таких как НАД.
Основные отличия дихотомического анаэробного распада глюкозы и аэробного гликолиза
Аэробный распад глюкозы можно выразить суммарным уравнением:
С6Н12О6 + 6О2 → 6СО2 + Н2О + 2880 кДж/моль.
Этот процесс включает несколько стадий:
1. Аэробный гликолиз — процесс окисления глюкозы с образованием двух молекул пирувата; Аэробным гликолизом называют процесс окисления глюкозы до пировиноградной кислоты, протекающий в присутствии кислорода. Все ферменты, катализирующие реакции этого процесса, локализованы в цитозоле клетки.
2. Общий путь катаболизма, включающий превращение пирувата в ацетил-КоА и его дальнейшее окисление в цитратом цикле;
3. Цепь переноса электронов на кислород, сопряжённая с реакциями дегидрирования, происходящими в процессе распада глюкозы.
Анаэробным гликолизом называют процесс расщепления глюкозы с образованием в качестве конечного продукта лактата. Этот процесс протекает без использования кислорода и поэтому не зависит от работы митохондриальной дыхательной цепи.
АТФ образуется за счёт реакций субстратного фосфорилирования.
Суммарное уравнение процесса:
С6Н1206 + 2Н3Р04 + 2АДФ = 2С3Н6О3 + 2АТФ + 2Н2O.
Реакции анаэробного гликолиза
При анаэробном гликолизе (рис.14) в цитозоле протекают все 10 реакций, идентичных аэробному гликолизу. Лишь 11-я реакция, где происходит восстановление пирувата цитозольным NADH, является специфической для анаэробного гликолиза (рис.15).
Восстановление пирувата в лактат катализирует лактатдегидрогеназа (реакция обратимая, и фермент назван по обратной реакции). С помощью этой реакции обеспечивается регенерация NAD+ из NADH без участия митохондриальной дыхательной цепи в иситуациях, связанных с недостаточным снабжением клеток кислородом.
Роль акцептора водорода от NADH (подобно кислороду в дыхательной цепи) выполняет пируват. Таким образом, значение реакции восстановления пирувата заключается не в образовании лактата, а в том, что данная цитозольная реакция обеспечивает регенерацию NAD+.
К тому же лактат не является конечным продуктом метаболизма, удаляемым из организма. Это вещество выводится в кровь и утилизируется, превращаясь в печени в глюкозу, или при доступности кислорода превращается в пируват, который вступает в общий путь катаболизма, окисляясь до СО2 и Н2О.
Фаза 2. Синтез Адезинтрифосфата
В данной фазе гликолиза будет аккумулироваться в виде АТФ биохимическая энергия. Адезинтрифосфат образуется из адезиндифосфата за счет фосфорилирования. А также образуется НАДН.
Аббревиатура НАДН имеет очень сложную и труднозапоминаемую для неспециалиста расшифровку – Никотинамидадениндинуклеотид. НАДН – это кофермент, небелковое соединение, участвующее в химических процессах живой клетки. Он существует в двух формах:
- окисленной (NAD+, NADox);
- восстановленной (NADH, NADred).
В обмене веществ NAD принимает участие в окислительно-восстановительных реакциях транспортируя электроны из одного химического процесса в другой. Отдавая, или принимая электрон, молекула преобразуется из NAD+ в NADH, и наоборот. В живом организме НАД вырабатывается из триптофана или аспартата аминокислот.
Две микрочастицы глицеральдегид-3-фосфата подвергаются реакциям, в ходе которых образуется пируват, и 4 молекулы АТФ. Но конечный выход адезинтрифосфата составит 2 молекулы, поскольку две затрачены в подготовительной фазе. Процесс продолжается.
6-я ступень – окисление глицеральдегид-3-фосфата
В данной реакции происходит окисление и фосфорилирование глицеральдегид-3-фосфата. В итоге получается 1,3-дифосфоглицериновая кислота. В ускорении реакции участвует глицеральдегид-3-фосфатдегидрогеназа

Реакция происходит при участии энергии, полученной извне, поэтому она называется эндергонической. Такие реакции протекают параллельно с экзергоническими, то есть выделяющими, отдающими энергию. В данном случае такой реакцией служит следующий процесс.
7-я ступень. Перемещение фосфатной группы с 1,3-дифосфоглицерата на адезиндифосфат

В этой промежуточной реакции фосфорильная группа переносится фосфоглицераткиназой с 1,3-дифосфоглицерата на адезиндифосфат. В итоге получаются 3-фосфоглицерат и АТФ.
Фермент фосфоглицераткиназа приобрел свое название за способность катализировать реакции в обоих направлениях. Этот фермент также транспортирует фосфатный остаток с адезинтрифосфата на 3-фосфоглицерат.
6-я и 7-я реакции часто рассматриваются как единый процесс . 1,3-дифосфоглицерат в нем рассматривается как промежуточный продукт. Вместе 6-я и 7-я реакции выглядят так:
Глицеральдегид-3-фосфат+ADP+Pi +NAD+⇌3 -фосфоглицерат+ATP+NADH+Н+,ΔG′о = −12,2 кДж/моль.
И суммарно эти 2 процесса освобождают часть энергии.
8-я ступень. Перенесение фосфорильной группы с 3-фосфоглицерата.

Получение 2-фосфоглицерата – процесс обратимый, происходит под каталитическим действием фермент фосфоглицератмутазы. Фосфорильная группа переносится с двухвалентного атома углерода 3-фосфоглицерата на трехвалентный атом 2-фосфоглицерата, в итоге образуется 2-фосфоглицериновая кислота. Реакция проходит при участи положительно заряженных ионов магния.
9-я ступень. Выделение воды из 2-фосфоглицерата
Эта реакция в своей сути является второй реакцией расщепления глюкозы (первой была реакция 6-й ступени). В ней фермент фосфопируватгидратаза стимулирует отщепление воды от атома С, то есть процесс элиминирования из молекулы 2-фосфоглицерата и образование фосфоенолпирувата (фосфоенолпировиноградной кислоты).

10-я и последняя ступень. Перенос фосфатного остатка с ФЕП на АДФ
В заключительной реакции гликолиза задействованы коферменты – калий, магний и марганец, в качестве катализатора выступает фермент пируваткиназа.

Преобразование енольной формы пировиноградной кислоты в кето-форму является обратимым процессом, и в клетках присутствуют оба изомера. Процесс перехода изометрических веществ из одного в другой называется таутомеризацией.
Что такое гликолиз
В общих чертах, гликолиз — это процесс, который происходит в цитоплазме всех клеток: от низших бактерий до высших млекопитающих — людей. Для некоторых это единственный метаболический путь доставки энергии клетке — например, для бактерий, для других же это метаболический путь, в который «сливаются» и другие метаболиты — белки и липиды.
Гликолиз — это основной путь расщепления глюкозы в нашем организме, основное биологическое значениеэтого процесса заключается в получении энергии и других продуктов обмена.
 Гликолиз происходит как в аэробных, так и в анаэробных условиях. Процесс в анаэробных условиях (недостаток кислорода) называется анаэробным гликолизом — конечным продуктом лактата и ферментации в дрожжах — алкогольной или молочнокислой ферментации.
Гликолиз происходит как в аэробных, так и в анаэробных условиях. Процесс в анаэробных условиях (недостаток кислорода) называется анаэробным гликолизом — конечным продуктом лактата и ферментации в дрожжах — алкогольной или молочнокислой ферментации.
При наличии кислорода этот процесс называется аэробным гликолизом — конечным продуктом выступают CO2 и H2O,
Гликолиз представляет собой серию реакций, в которых одна молекула глюкозы распадается на две молекулы пирувата. Но так происходит не всегда, в случаях когда доступ кислорода в этой реакции затруднен, проще говоря, в анаэробных условиях, то пируват превращается в лактат или спирт.
Механизмы анаэробного метаболизма: гликолиз в анаэробных условиях
В анаэробных условиях O2 отсутствует. Отсутствие конечного субстрата O2 ингибирует активность дыхательных структур (до этого они неактивны), и таким образом конечным продуктом распада глюкозы в анаэробных условиях является лактат,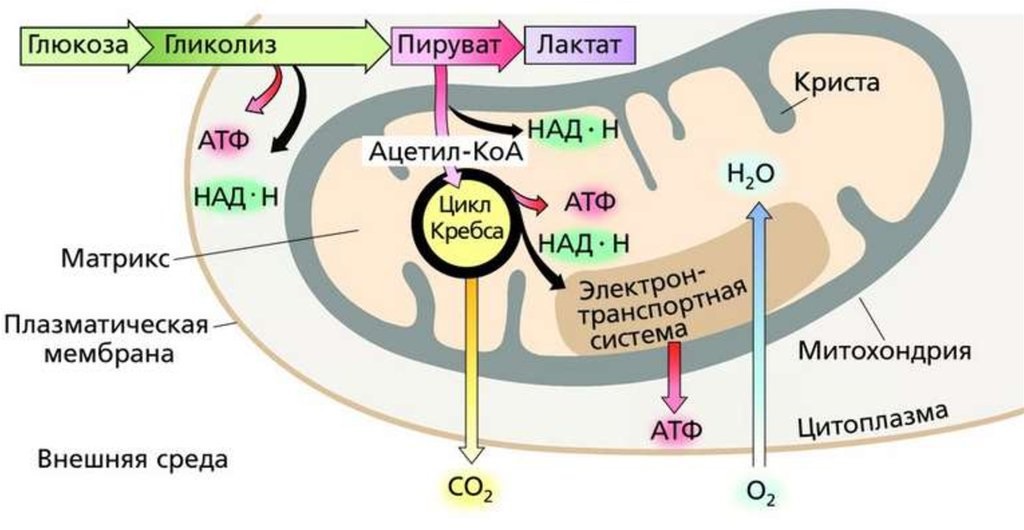
Анаэробный распад глюкозы в физиологических условиях наблюдается в эритроцитах (без митохондрий) и в сильно сокращающихся мышцах (недостаточное кровоснабжение кислородом), это наблюдается при сильной физической работе — присутствует истощение O2 в мышечных клетках (в форме оксимиоглобина).
Лактат в мышечных клетках приводит к мышечной лихорадке, которая преодолевается неинтенсивной мышечной активностью, направленной на полное расщепление лактата в мышцах, до CO2 , H2O и H2 в результате аэробного гликолиза.
При патологических состояниях и онкологических заболеваниях, у многих людей наблюдается так называемый эффект Пастера, при котором клетки из-за уменьшенного поступления крови или кислорода переключаются на анаэробный распад глюкозы, связанный с повышенным ее потреблением (повышенная экспрессия трансмиттеров глюкозы GLUT1 ) и гипогликемией.
Анаэробный гликолиз, как при физиологических, так и при патологических состояниях, характеризуется повышенным уровнем конечного продукта в результате расщепления его лактата в плазме крови — лактатемией, что может привести к ацидозу.
Дальнейшее расщепление лактата
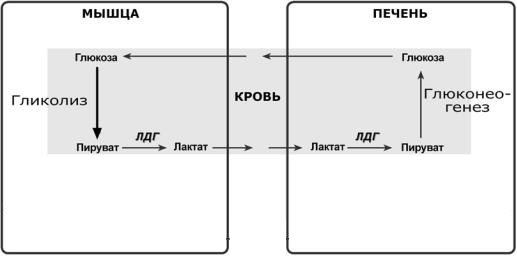
Лактат метаболизируется из печени в пируват, катализируя реакцию в обратном направлении, и глюкоза синтезируется пируватом с использованием ферментов глюконеогенеза в печени через цикл Кори (лактатный цикл).
Вот в этой схеме и кроется ответ на вопрос о том, как влияет анаэробный гликолиз на производство энергии, ведь мы видим, что наша молочная кислота, образовавшаяся в мышцах, через кровь попадает в печень и участвует в процессе глюконеогенеза — создания глюкозы из неуглеводных продуктов.
Что такое анаэробный гликолиз?
Наряду с аэробным гликолизом, то есть расщеплением глюкозы при участии О2 , существует и так называемый анаэробный распад глюкозы, в котором кислород не участвует. Он также состоит из десяти последовательных реакций. Но где протекает анаэробный этап гликолиза, связан ли он с процессами кислородного расщепления глюкозы, или это самостоятельный биохимический процесс, попробуем в этом разобраться.
Анаэробный гликолиз – это распад глюкозы при отсутствии кислорода с образованием лактата. Но в процессе образования молочной кислоты НАДН в клетке не накапливается. Этот процесс осуществляется в тех тканях и клетках, которые функционируют в условиях кислородного голодания – гипоксии. К таким тканям в первую очередь относятся скелетные мышцы. В эритроцитах, несмотря на наличие кислорода, тоже в процессе гликолиза образуется лактат, потому что в кровяных клетках отсутствуют митохондрии.
Анаэробный гидролиз протекает в цитозоле (жидкой части цитоплазмы) клеток и является единственным актом, продуцирующим и поставляющим АТФ, поскольку в данном случае окислительное фосфорилирование не работает. Для окислительных процессов нужен кислород, а его в анаэробном гликолизе нет.
И пировиноградная, и молочная кислоты служат источниками энергии, для выполнения мышцами определенных задач. Излишки кислот поступают в печень, где под действием ферментов снова превращаются в гликоген и глюкозу. И процесс начинается снова. Недостаток глюкозы восполняется питанием – употреблением сахара, сладких фруктов, и иных сладостей. Так что нельзя в угоду фигуре совсем отказываться от сладкого. Сахарозы нужны организму, но в меру.
